दोस्तों यहां पर क्लास 10th साइंस का क्वेश्चन आंसर (Class 10th Science Objective & Subjective Question Answer) दिया गया है तथा यहां पर क्लास 10th साइंस का मॉडल पेपर (Class 10th Science Model Paper 2023) तथा ऑनलाइन टेस्ट (Class 10th Science Online Test) भी दिया गया है वैसे विद्यार्थी जो मैट्रिक परीक्षा 2023 की तैयारी कर रहे हैं तो इस पेज में आपको क्लास 10th साइंस का सब्जेक्टिव धातु एवं अधातु का लघु उत्तरीय प्रश्न उत्तर ( Dhaatu evan Adhaatu Subjective Question Answer ) यहां पर दिया गया है तथा अगर आप लोग धातु एवं अधातु का ऑब्जेक्टिव क्वेश्चन आंसर पढ़ना चाहते हैं तो लिंक पर क्लिक करके पढ़ सकते हैं
| Bihar Board Daily Online Test Class Xth |
|
| Click Here |
|
| Click Here |
|
-
Class 10th Science (विज्ञान) VVI Guess Paper Question Answer 2023
| S.N | Science (विज्ञान) 📒 |
| 1. | Physics (भौतिक बिज्ञान) Guess Paper |
| 2. | Chemistry (रसायन शास्त्र) Guess Paper |
| 3. | Biology (जिव-विज्ञान) Guess Paper |
धातु एवं अधातु का सब्जेक्टिव प्रश्न उत्तर 2023
| 2 अंक स्तरीय प्रश्न |
1. निष्क्रिय गैसों के नाम लिखिए।
उत्तर ⇒ He, Ne, Ar, Kr, Xe, Rn
2. टांके (सोल्डर) के अवयव घटक लिखें।
उत्तर ⇒ सीसा (50%) तथा टिन (50%)।
3. Zn, Al, Mg एवं Fe दिए गए धातुओं को घटते अभिक्रियात्मकता क्रम में लगाएँ।
उत्तर ⇒ Mg > Al > Zn > Fe
4. कुल 22 अधातुओं में से कितनी ठोस, तरल तथा गैसीय हैं ?
उत्तर ⇒ 22 अधातुओं में से 11 गैसें हैं, एक तरल है तथा शेष 10 ठोस हैं।
5. उपधातु किसे कहते हैं ? उदाहरण सहित समझाइए।
उत्तर ⇒ उपधातु वे तत्व हैं जिनमें धातु एवं अधातु दोनों के गुण हैं।
जैसे- आर्सेनिक (As), एंटीमनी (Sb), बिस्मथ (Bi)
6. सोडियम को खुले में क्यों नहीं रख सकते ?
उत्तर ⇒ सोडियम वायु के संपर्क में आने पर तेजी से अभिक्रिया करता है। इसलिए इसे खुले में नहीं रखा जाता।
7. जर्मन सिल्वर के अवयव घटक लिखें।
उत्तर ⇒ तांबा, निकिल तथा जिंक।
8. मैग्नेलियम के अवयव घटक लिखें।
उत्तर ⇒ एल्युमिनियम (94.7%) तथा मैग्नीशियम (5.3%)।
9. आयनिक यौगिक कठोर क्यों होते हैं ?
उत्तर ⇒ धनात्मक एवं ऋणात्मक आयनों के बीच मजबूत आकर्षण बल के कारण आयनिक यौगिक ठोस एवं थोड़े कठोर होते हैं ।
10. कांसे के अवयव घटक लिखें।
उत्तर ⇒ तांबा तथा टिन (कलई)।
Class 10th Chemistry Dhaatu evan Adhaatu Subjective question answer 2023
11. मिश्रधातु क्या होते हैं ?
उत्तर ⇒ दो या दो से अधिक धातुओं या एक धातु तथा अधातु का समांगी मिश्रण मिश्रधातु कहलाता है।
12. तीन धातुओं के नाम बताइए जो प्रकृति में मुक्त अवस्था में पाई जाती हैं।
उत्तर ⇒ सोना (Au), सिल्वर (Ag), तथा प्लैटिनम (Pt) है।
13. लोहे को जंग से बचाने के लिए दो तरीके बताइए।
उत्तर ⇒ लोहे को जंग से बचाने के लिए निम्न तरीके हैं –
I. लोहे की वस्तुओं पर पेंट करके।
II. लोहे की वस्तुओं पर जिंक आदि की परत चढ़ाकर।
14. नाइट्रोजन के ऑक्साइड के नाम लिखें।
उत्तर ⇒ N₂O, NO एवं NO₂ नाइट्रोजन के तीन ऑक्साइड हैं।
15. जिंक को आयरन (II) सल्फेट के विलयन में डालने से क्या होता है ? इसकी रासायनिक अभिक्रिया लिखिए।
उत्तर ⇒ जिंक (Zn), आयरन (II) से अधिक क्रियाशील है। अतः जिंक आयरन (II) सल्फेट के विलयन से आयरन को विस्थापित कर देता है।
Zn + FeSO₄ + ZnSO₄ + Fe
16. अभिक्रियाशील धातु को तनु हाइड्रोक्लोरिक अम्ल में डाला जाता है तो कौन-सी गैस निकलती है? आयरन के साथ तनु H₂SO₄ की रासायनिक अभिक्रिया लिखिए।
उत्तर ⇒ अभिक्रियाशील धातु को तनु हाइड्रोक्लोरिक अम्ल में डाला जाता है तो हाइड्रोजन गैस (H₂) उत्पन्न करती है।
Fe+ 2HCl → FeCl₂ + H₂
Fe+ H₂SO₄ → FeSO₄ + H₂
17. संक्षारण की शतों को लिखिए ?
उत्तर ⇒ संक्षारण की शर्ते निम्नलिखित हैं –
(i) वायु की उपस्थिति।
(ii) नमी की उपस्थिति।
(iii) अभिक्रियाशील धातु की उपस्थिति।
18. अशुद्ध ताँबा में विधुत अपघटनी परिष्करण में प्रयुक्त ऐनोड, कैथोड तथा विधुत अपघट्य के नाम लिखें ?
उत्तर ⇒ अशुद्ध ताँबा ऐनोड, शुद्ध ताँबा कैथोड और अम्लीय CuSO₄ का विलयन विधुत अपघट्य का कार्य करता है।
19. किसी धातु M के विधुत अपघटनी परिष्करण में आप ऐनोड, कैथोड एवं विधुत अपघट्य किसे बनाएँगे ?
उत्तर ⇒ एनोड : अशुद्ध धातु M की एक मोटी छड़।
कैथोड : शुद्ध धातु की पतली-सी छड़।
विधुत अपघट्य : धातु के किसी लवण का जलीय विलयन।
20. प्रत्युस ने सल्फर चूर्ण को स्पैचुला में लेकर उसे गर्म किया। चित्र के अनुसार एक परखनली को उलटा करके उसने उत्सर्जित गैस को एकत्र किया।
(a) गैस की क्रिया क्या होगी
(i) सूखे लिटमस पत्र पर?
(ii) आर्द्र लिटमस पत्र पर ?
(b) ऊपर की अभिक्रियाओं के लिए संतुलित रासायनिक अभिक्रिया लिखिए।
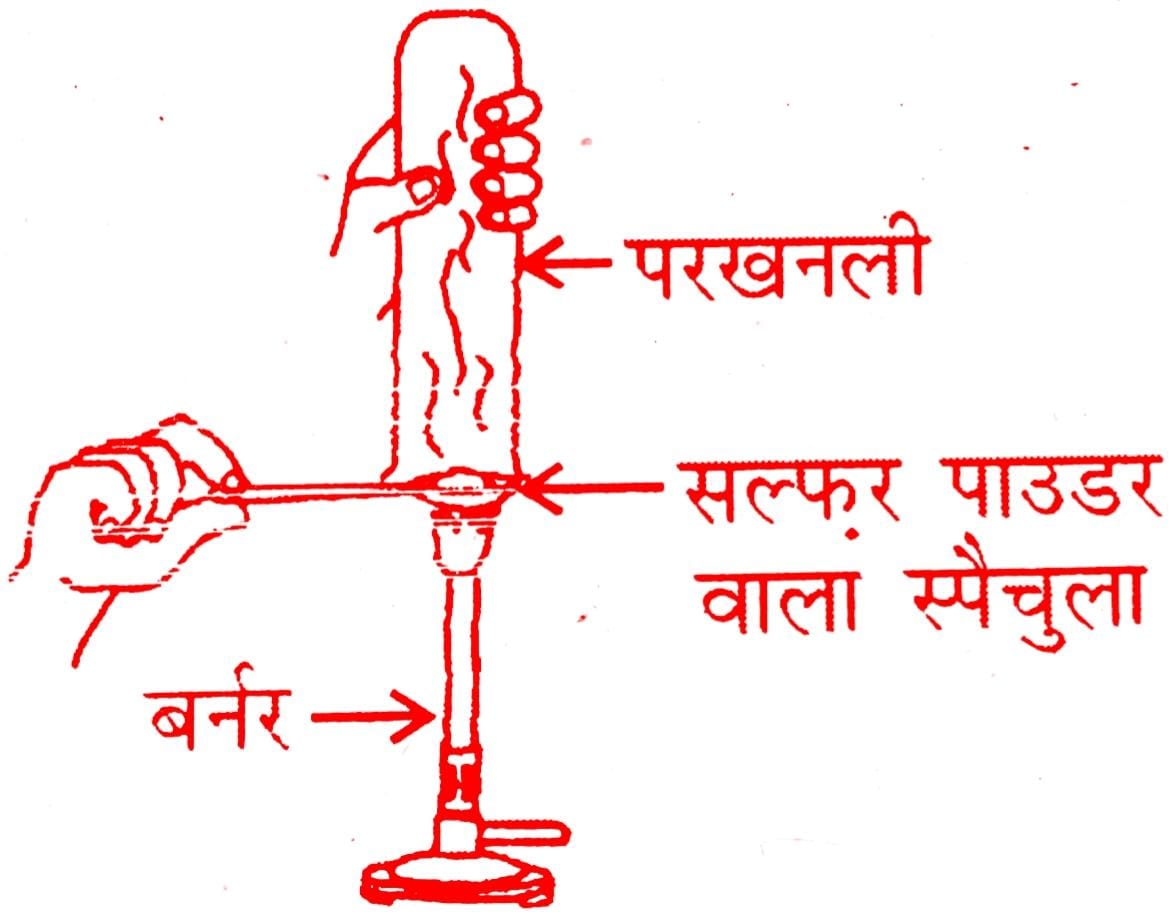
उत्तर ⇒ (a)
(i) शुष्क लिटमस पर कोई प्रभाव नहीं पड़ेगा।
(ii) आर्द्र लिटमस लाल हो जाएगा।
(b) S+O₂ → SO₂
Dhaatu evan Adhaatu class 10th Laghu Uttareey Prashn uttar pdf download
21. ऐसी धातु का उदाहरण दीजिए जो
(i) कमरे के ताप पर द्रव होती है।
(ii) चाकू से आसानी से काटा जा सकता है।
(iii) ऊष्मा की सबसे अच्छी चालक होती है।
(iv) ऊष्मा की कुचालक होती है।
उत्तर ⇒ (i) पारा [Hg]
(ii) सोडियम [Na]
(iii) सिल्वर/चाँदी [Ag]
(iv) पारा और सीसा [Hg और Pb]
22. इन अभिक्रियाओं के लिए समीकरण लिखिए –
(i) भाप के साथ आयरन।
उत्तर ⇒ 3Fe(s) +4H₂O(g) → Fe₃O₄(s) + 4H₂ (g)
(ii) जल के साथ कैल्सियम तथा पोटैशियम
उत्तर ⇒ Ca(s) + 2H₂O(l) → Ca(OH)₂ (aq) + H₂ (g)
2K(s) + 2H₂O(1) → 2KOH(aq) + H₂ (g) + ऊष्मीय ऊर्जा
23. आयनिक यौगिकों का गलनांक उच्च क्यों होता है ?
उत्तर ⇒ आयनिक यौगिक ठोस एवं कठोर होते हैं। ऐसा आयनों के बीच मजबूत अन्तर-आयनिक आकर्षण बल के कारण होता है। इस आकर्षण बल को कम करने के लिए अत्यधिक मात्रा में ऊर्जा की आवश्यकता होती है। यही कारण है कि आयनिक यौगिकों का गलनांक उच्च होता है।
24. निम्न पदों की परिभाषा दीजिए –
(i) खनिज (ii) अयस्क (iii) गैंग
उत्तर ⇒ परिभाषा निम्नलिखित हैं –
(i) खनिज : पृथ्वी की परत में विद्यमान धातु-युक्त ठोस पदार्थ (तत्त्व या यौगिक) खनिज कहलाते हैं।
(ii) अयस्क : जिस खनिज से धातु प्राप्त करना सरल तथा आर्थिक रूप से लाभदायक हो उसे अयस्क कहते हैं।
(iii) गैंग : अयस्क में विद्यमान अशुद्धियों को गैंग कहते हैं।
25. धातु को उसके ऑक्साइड से प्राप्त करने के लिए किस रासायनिक प्रक्रम का उपयोग किया जाता है ?
उत्तर ⇒ कम क्रियाशील धातु के ऑक्साइडों को केवल गर्म करके संगत धातुओं में अपचयित करते हैं।

सक्रिय श्रेणी के बीच में स्थित धातुओं में ऑक्साइडों को कार्बन के साथ गर्म करके धातुओं में अपचयित करते हैं।
![]()
इसे अपचयी क्रिया कहते हैं।
26. आपने ताँबे के मलीन बर्तन को नींबू या इमली के रस से साफ करते अवश्य देखा होगा। यह खट्टे पदार्थ बर्तन को साफ करने में क्यों प्रभावी हैं ?
उत्तर ⇒ कॉपर को आर्द्र वायु में खुला छोड़ देने पर एक हरे रंग का क्षारीय कॉपर कार्बोनेट परत बन जाती है। नींबू अथवा इमली जैसे खट्टे पदार्थों में अम्ल होता है। यह अम्ल क्षारीय कॉपर कार्बोनेट को उदासीन कर देता है। जिससे कॉपर पात्र फिर से चमकदार दिखाई देने लगता है।
Dhaatu evan Adhaatu class 10th Subjective Laghu Uttareey Question Answer
27. गर्म जल का टैंक बनाने में ताँबे का उपयोग होता है परंतु इस्पात (लोहे की मिश्रातु) का नहीं। इसका कारण बताइए।
उत्तर ⇒ आयरन की तुलना में कॉपर ऊष्मा की सुचालक है। कॉपर गर्म जल के साथ भी अभिक्रिया नहीं करता। परन्तु आयरन गर्म जल से अभिक्रिया करता है।
3Fe(s) + 4H₂O(1)→ Fe₃O. +4H₄O
28. दो धातुओं के नाम बताइए जो तनु अम्ल से हाइड्रोजन को विस्थापित कर देंगे तथा दो धातुएँ जो ऐसा नहीं कर सकती है।
उत्तर ⇒ तनु अम्लों से हाइड्रोजन विस्थापित करने वाली धातुएँ मैग्नीशियम (Mg) तथा एल्युमिनियम (Al), तनु अम्लों से हाइड्रोजन विस्थापित न करने वाली’ धातुएँ कॉपर (Cu) तथा सिल्वर (Ag) है।
29. सोडियम को किरोसिन में डुबो कर क्यों रखा जाता है ?
उत्तर ⇒ सोडियम (Na) बहुत क्रियाशील धातु है। यह सामान्य ताप पर भी नमी तथा ऑक्सीजन के साथ तेजी से अभिक्रिया करती है। अंत: इसे वायु में खुला छोड़ देने पर आग पकड़ लेता है। इसलिए सोडियम को किरोसीन तेल में डुबो कर रखा जाता है।
30. एक व्यक्ति प्रत्येक घर में सुनार बनकर जाता है। उसने पुराने एवं मलीन सोने के आभूषणों में पहले जैसी चमक पैदा करने का ढोंग रचाया। कोई संदेह किए बिना ही एक महिला अपने सोने के कंगन उसे देती है जिसे वह एक विशेष विलयन में डाल देता है। कंगन नए की तरह चमकने लगते हैं लेकिन उनका वजन अत्यंत कम हो जाता है। वह महिला बहुत दुखा होती है तथा तर्क-वितर्क के पश्चात उस व्यक्ति को झुकना पड़ता है। एक जासूस की तरह क्या आप विलयन की प्रकृति के बारे में बता सकते हैं। यदि हाँ, तो वर्णन कीजिए।
उत्तर ⇒ हाँ, सुनार द्वारा प्रयोग किया गया विलयन, एक्वारीजिया है। एक्वारीजिया विलयन में तनु हाइड्रोक्लोरिक अम्ल एवं नाइट्रिक अम्ल 3:1 के अनुपात में होता है। सोना एक्वारीजिया में घुलनशील है इसलिए महिला के कंगन का भार कम हो जाता है।
31. इलेक्ट्रॉन के स्थानांतरण के द्वारा Na₂O एवं MgO के निर्माण को दर्शाइए।
उत्तर ⇒ 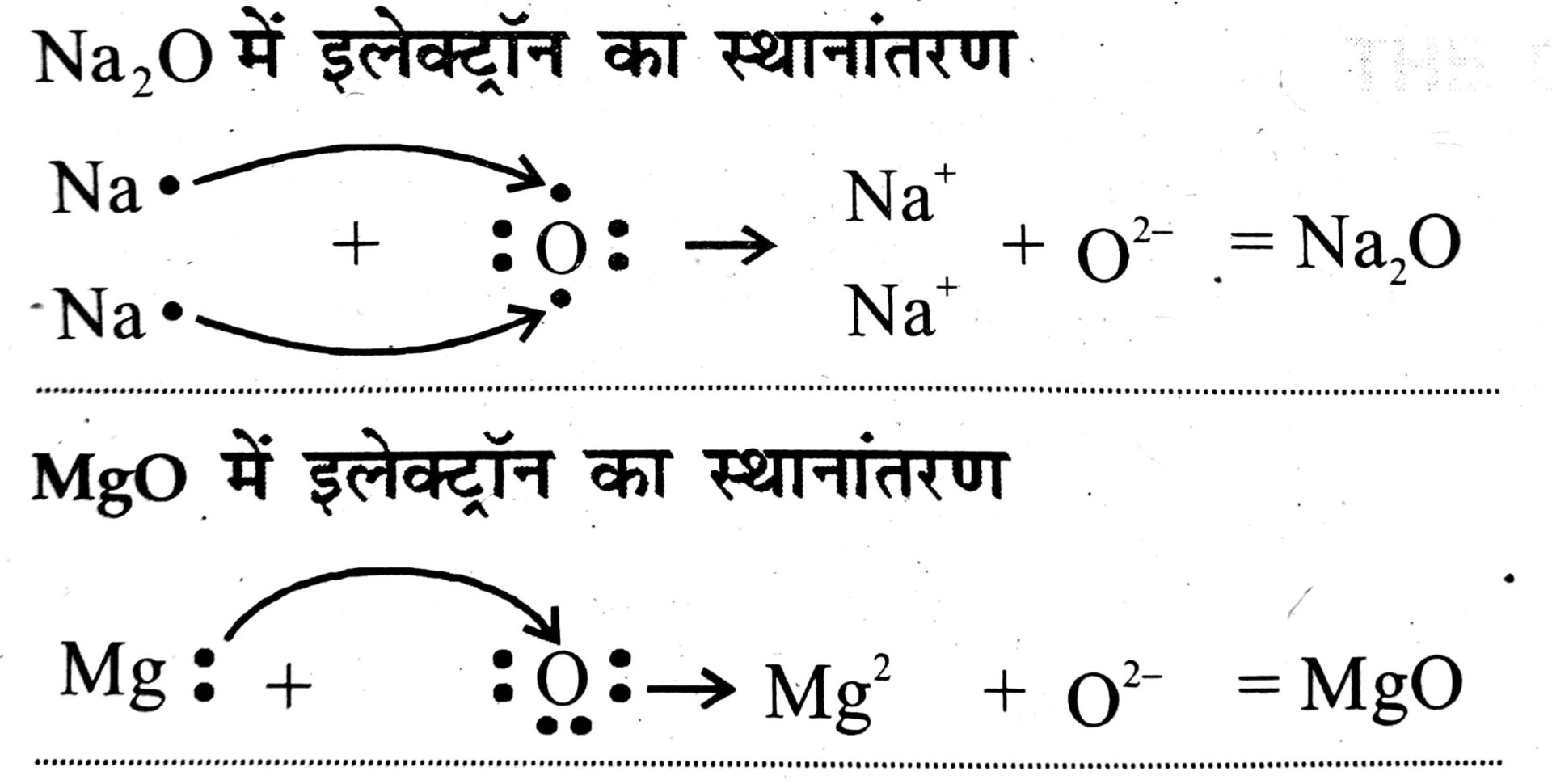
32. आघातवर्ध्य तथा तन्य का अर्थ बताइए।
उत्तर ⇒ आघातवर्ध्य : धातुओं का वह गुण जिसके द्वारा उन्हें पीट कर पतली चादरों में परिवर्तित किया जा सकता है। आघातवर्ध्य कहलाता है।
तन्य : धातुओं का वह गुण जिसके कारण उनके लंबे एवं पतले तार बनाए जा सकते हैं तन्य कहलाते हैं।
33. भर्जन (जारण) और निस्तापन में अंतर लिखिए ?
उत्तर ⇒ जारण और निस्तापन में निम्नलिखित अंतर है
जारण :
(i). इस प्रक्रिया में अयस्क को वायु की उपस्थिति में गर्म किया जाता है।
(ii). यह सल्फाइड अयस्कों के लिए प्रयुक्त होती है।
निस्तापन :
(i). इस अभिक्रिया में अयस्क को वायु की अनुपस्थिति में गर्म किया जाता है।
(ii) यह ऑक्साइड एवं कार्बोनेट अयस्कों के लिए प्रयुक्त होती है।
धातु एवं अधातु v.v.i Subjective Question Answer
34. विधुत ऋणात्मकता क्या है? सबसे अधिक विधुत ऋणात्मक तत्व का नाम लिखें।
उत्तर ⇒ किसी अणु में परमाणुओं की इलेक्ट्रॉन के बंधित जोडे को अपनी ओर खींचने की प्रवृत्ति को विधुत ऋणात्मकता कहते हैं। सबसे अधिक विधुत ऋणात्मक तत्व फ्लोरीन (F) है।
35. धातुएँ विधुत की सुचालक क्यों होती हैं? दो उदाहरण दीजिए।
उत्तर ⇒ धातु के परमाणुओं के बाह्यतम सेल में 1, 2 या 3 इलेक्ट्रॉन होते हैं जिसे मुक्त इलेक्ट्रॉन कहते हैं। धातुओं की चालकता उसमें उपस्थित मुक्त इलेक्ट्रॉन के कारण ही होता है। ये इलेक्ट्रॉन धातु से होकर दोड़ सकते हैं और ये विधुत का संवहन करते हैं।
36. एक द्रव धातु और एक द्रव अधातु का नाम लिखिए ?
उत्तर ⇒ द्रव धातु पारा है और द्रव अधातु ब्रोमीन है।
37. अधातुएँ विधुत की कुचालक क्यों होती है ? एक ऐसे अधातु के नाम बताएँ जो विधुत की सुचालक होती है ?
उत्तर ⇒ अधातुओं में मुक्त-इलेक्ट्रॉन नहीं होने के कारण ये विधुत के कुचालक होते हैं। विधुत के सुचालक एक अधातु ग्रेफाइट है, जो कार्बन का अपरूप है।
38. अधातु के चार भौतिक गुणों को लिखिए ?
उत्तर ⇒ अधातु के चार भौतिक गुण है –
(i) अधातु में धात्विक चमक नहीं होती है, अपवाद आयोडीन।
(ii) अधातु के गलनांक एवं क्वथनांक निम्न होते हैं।
(iii) अधातुएँ जल में अल्प घुलनशील होता है।
(iv) अधातुएँ आघातवर्ध्य या तन्य नहीं होता है।
39. धातुओं के चार भौतिक गुण लिखिए ?
उत्तर ⇒ धातुओं के चार भौतिक गुण –
(i) ये आघातवर्ध्य एवं तन्म होते हैं।
(ii) ये ऊष्मा के सुचालक होते हैं।
(iii) इनमें विशेष चमक पाई जाती है।
(iv) इनके गलनांक एवं क्वथनांक उच्च होते हैं।
40. कार्बन डाइऑक्साइड (CO₂) को इलेक्ट्रॉन बिंदु संरचना क्या होगी ?
उत्तर ⇒ 
धातु एवं अधातु सब्जेक्टिव लघु उत्तरीय प्रश्न उत्तर
41. अधातु किसे कहते हैं ? दो अधातुओं के नाम बताइए।
उत्तर ⇒ ऐसे तत्व जो इलेक्ट्रॉनों को ग्रहण कर ऋणायन प्रदान करते हैं, उसे अधातु कहते हैं। उदाहरण- कार्बन और सल्फर।
42. धातु किसे कहते हैं ? दो उदाहरण दीजिए।
उत्तर ⇒ ऐसे तत्व जो इलेक्ट्रॉन का त्याग कर धनायन प्रदान करते हैं, उसे धातु कहते हैं। उदाहरण- लोहा और चाँदी।
43. आयन किसे कहते हैं? यह कितने प्रकार के होते हैं।
उत्तर ⇒ विधुत आवेशित परमाणु या परमाणुओं के समूह को आयन कहते हैं। ये दो प्रकार के होते हैं –
(i) धनायन (ii) ऋणायन
44. आयनिक यौगिक किसे कहते हैं ? आयनिक यौगिक का दो उदाहरण दीजिए।
उत्तर ⇒ धातु से अधातु में इलेक्ट्रॉन के स्थानांतरण से बने यौगिकों को आयनिक यौगिक या वैद्युत संयोजक यौगिक कहते हैं।
उदाहरण- NaCl, MgCl₂
45. आयनिक यौगिकों का द्रवनांक एवं क्वथनांक उच्च होते हैं क्यों ?
उत्तर ⇒ आयनिक यौगिकों का द्रवनांक एवं क्वथनांक उच्च होते हैं क्योंकि धन एवं ऋण आयनों के बीच काफी मजबूत आकर्षण बल होता है। फलतः उनके आकर्षण बल को तोड़ने के लिए ऊर्जा की अधिक मात्रा की आवश्यकता होती है।
46. Na₂O एवं MgO यौगिकों में कौन से आयन उपस्थित हैं ?
उत्तर ⇒ Na₂O में उपस्थित आयन Na+ एवंO²- Mgo में उपस्थित आयन Mg²+ + एवं O²-
47. निम्नलिखित का इलेक्ट्रॉनिक विन्यास लिखिए ?
I. सोडियम
II. सोडियम आयन
III. कैल्सियम
IV. क्लोरीन
उत्तर ⇒ सोडियम (Na) का इलेक्ट्रानिक विन्यास- 2, 8, 1
सोडियम (Na+) आयन का इलेक्ट्रॉनिक विन्यास- 2, 8
कैल्सियम (Ca) का इलेक्ट्रॉनिक विन्यास- 2,8, 8, 2
क्लोरीन (Cl) का इलेक्ट्रॉनिक विन्यास- 2, 8,7
48. निम्न तत्वों के संकेत, परमाणु संख्या और इलेक्ट्रॉनिक विन्यास लिखिए ?
I. फासफोरस
II. ऑक्सीजन
III. पोटैशियम
IV. मैग्नेशियम
उत्तर ⇒
| तत्व | संकेत | परमाणु सं० | इलेक्ट्रोनिक विन्यास |
| फास्फोरस | P | 15 | 2, 8, 5 |
| ऑक्सीजन | O | 8 | 2,6 |
| पोटेशियम | K | 19 | 2, 8, 8, 1 |
| मैग्नेशियम | Mg | 12 | 2, 8, 2 |
49. लोहा के वस्तुओं का जस्तीकरण क्यों किया जाता है ?
उत्तर ⇒ जिंक लोहा से अधिक अभिक्रियाशील है। जिंक का गलनांक लोहा से कम होता है और यह उच्च तापमान को सहन कर सकता है। इसीलिए जंग से बचाने के लिए ही लोहा के वस्तुओं का जस्तीकरण किया जाता है।
50. अमलगम तथा जंग को परिभाषित करें ?
उत्तर ⇒ अमलगम : यदि मिश्रधातु में एक धातु पारा हो तो मिश्रधातु को अमलगम कहते हैं।
जंग : जब लोहा को अधिक समय तक आर्द्र हवा में छोड़ दिया जाता है तो उस पर भूरे रंग की एक परत जम जाती है, जिसे जंग कहते हैं।
Class 10th Science (Chemistry) Subjective Question 2023 (लघु उत्तरीय प्रश्न )
| रसायन विज्ञान ( CHEMISTRY ) लघु उत्तरीय प्रश्न | |
| 1. | रासायनिक अभिक्रियाएं एवं समीकरण |
| 2. | अम्ल क्षार एवं लवण |
| 3. | धातु एवं अधातु |
| 4. | कार्बन और उसके यौगिक |
| 5. | तत्वों का वर्गीकरण |
Class 10th Science (Chemistry) Subjective Question 2023 (दीर्घ उत्तरीय प्रश्न )
| S.N | Class 10th Chemistry (रसायन विज्ञान दीर्घ उत्तरीय प्रश्न) |
| 1. | रासायनिक अभिक्रियाएं एवं समीकरण |
| 2. | अम्ल क्षार एवं लवण |
| 3. | धातु एवं अधातु |
| 4. | कार्बन और उसके यौगिक |
| 5. | तत्वों का वर्गीकरण |
| Bihar Board Daily Online Test Class Xth |
|
| Click Here |
|
| Click Here |
|
![[ रासायन विज्ञान ] कक्षा-10 विज्ञान (रसायन विज्ञान) पाठ-03 धातु एवं अधातु सब्जेक्टिव क्वेश्चन आंसर 2023, धातु एवं अधातु सब्जेक्टिव लघु उत्तरीय प्रश्न उत्तर, धातु एवं अधातु का सब्जेक्टिव प्रश्न उत्तर 2023, Dhaatu evan Adhaatu ka Subjective Question Answer 2023, धातु एवं अधातु का महत्वपूर्ण सब्जेक्टिव प्रश्न, कक्षा -10 रासायन विज्ञान पाठ-3 धातु एवं अधातु लघु उत्तरीय प्रश्न, Class 10th Chemistry Dhaatu evan Adhaatu Subjective question answer 2023, Bihar board class 10th science Subjective question answer 2023, class 10th Dhaatu evan Adhaatu ka Subjective question answer, धातु एवं अधातु v.v.i Subjective Question Answer, धातु एवं अधातु क्वेश्चन आंसर, Dhaatu evan Adhaatu ka Subjective Question, Dhaatu evan Adhaatu class 10th question answer 2023, Bihar Board Class 10th रासायनिक अभिक्रिया एवं समीकरण Subjective Question 2023, धातु एवं अधातु क्लास 10th Notes, धातु एवं अधातु लघु उत्तरीय प्रश्न उत्तर, Dhaatu evan Adhaatu Question Answer Class 10th Science Matric Exam 2023, धातु एवं अधातु सब्जेक्टिव लघु उत्तरीय प्रश्न उत्तर, धातु एवं अधातु के प्रश्न उत्तर pdf, Dhaatu evan Adhaatu class 10th Subjective Laghu Uttareey Question Answer, Dhaatu evan Adhaatu class 10th Laghu Uttareey Prashn uttar pdf download, Dhaatu evan Adhaatu class 10th numerical, धातु एवं अधातु कक्षा 10 pdf,](https://pragatishilclasses.com/wp-content/uploads/2022/05/WhatsApp-Image-2022-05-13-at-12.30.56-PM-1024x576.jpeg)